文章來(lái)源:H. Pahlevaninezhad , A. M. D. Lee , C. Hyun - Spie Bios – 2013 Proc. of SPIE Vol. 8565 85652S-2
本文以實驗結合光學軟件FRED來(lái)驗證熒光介質上(shàng)覆蓋散射層的影(yǐng)響,結合AF-OCT系統能夠減少(shǎo)由于上(shàng)皮組織增厚引起的假陽性,增強AF疾病檢測的功效。
摘要:
在本文中,我們通(tōng)過模拟組織的自發熒光(AF)特性進行(xíng)了模型的研究。我們組合了光學相幹斷層掃描(OCT)和(hé)AF成像系統,依據散射層的厚度和(hé)濃度來(lái)測量AF信号的強度。使用由生(shēng)成的OCT圖像計(jì)算(suàn)得(de)到的厚度和(hé)散射濃度,結合AF-OCT系統能夠估計(jì)由上(shàng)皮組織散射引起的AF損耗。我們定義了一個(gè)校(xiào)正因子來(lái)計(jì)算(suàn)上(shàng)皮組織中的散射損耗,并且計(jì)算(suàn)了一個(gè)校(xiào)正散射AF信号。我們認為(wèi)校(xiào)正散射AF将會(huì)減少(shǎo)在早期呼吸道(dào)病變檢測中的診斷誤檢率,誤檢是由混合因子産生(shēng),如增加的皮層厚度和(hé)炎症。
關鍵詞:光學相幹斷層掃描;自發熒光;光散射;模型;光線光學;OCT A-line數(shù)據
1. 簡介
自發熒光(AF)成像是一項已實現的技(jì)術(shù),使用藍(lán)光來(lái)激發自然組織熒光。通(tōng)過收集高(gāo)風險區(qū)域進行(xíng)活檢識别,已經證明(míng)這項技(jì)術(shù)對于癌症的早期檢測和(hé)癌的分期是及其有(yǒu)效的。雖然通(tōng)過白光成像可(kě)以容易的檢測浸潤癌,原位癌和(hé)高(gāo)度的癌前病變的檢測卻十分棘手。白光成像中的變化十分微小(xiǎo),然而,AF成像可(kě)以清楚地對比這種病變。當受到藍(lán)光照射時(shí),正常的組織會(huì)發出強烈的綠色AF,而異常組織則缺少(shǎo)這種AF輻射。
盡管AF成像可(kě)以方便的檢測原位癌,對于良性組織的異常現象也是十分敏感的。例如,上(shàng)皮組織的厚度未必就與癌症相關,但(dàn)是它确實減少(shǎo)了由散射産生(shēng)的AF信号,導緻了假陽性。因此,将癌症與其他非危險異常現象區(qū)别開(kāi)來(lái)可(kě)以極大(dà)地增加治療的療效。
光學相幹斷層掃描(OCT)是可(kě)以獲得(de)生(shēng)物組織皮下圖像的一項相幹技(jì)術(shù),它可(kě)以提供小(xiǎo)于10μm軸向分辨率和(hé)大(dà)約3mm穿透深度的圖像。OCT采用了非電(diàn)離,通(tōng)常是近紅外的輻射來(lái)捕獲組織形态的實時(shí)圖像。OCT可(kě)以用于研究高(gāo)風險的組織位置。因此,當用于組合時(shí),以一種同時(shí)和(hé)協作(zuò)的形式,AF-OCT成像可(kě)以提供豐富的生(shēng)化信息,并定位組織形态,這些(xiē)不能通(tōng)過單獨的成像模式獲得(de)。比如,在上(shàng)皮組織增厚的情況下,OCT可(kě)以直接測量上(shàng)皮組織厚度,并且将AF信号衰減歸因于上(shàng)皮增厚,而不是癌症前期引起的膠原重建。因此,由OCT給定結構信息,并結合AF-OCT可(kě)以減少(shǎo)AF假陽性。
AF信号強度不僅取決于原位的熒光,也取決于不同組織層的光吸收和(hé)散射。組織的光散射已經經過了深入的研究1-6。模拟組織散射可(kě)以提供與AF信号強度有(yǒu)價值的信息。由于價格低(dī)廉、方便校(xiào)準且易于獲得(de),英脫利匹特(Intralipid)是用于組織模型最常見的散射媒介。這項工作(zuò)的目的是根據散射層的厚度模拟組織自發熒光的性質。我們定義了一個(gè)AF信号校(xiào)正因子,用來(lái)說明(míng)散射層引起的損耗。OCT圖像給出了散射層厚度和(hé)散射顆粒的濃度,這是校(xiào)正因子計(jì)算(suàn)所需的兩個(gè)因素。因此,我們提出了AF-OCT系統,作(zuò)為(wèi)癌症檢測的一個(gè)更靈敏和(hé)精确的成像工具。
首先,我們解釋了Intralipid模型研究,旨在模拟不同上(shàng)皮厚度的組織散射特性。然後,使用光線光學仿真來(lái)驗證實驗結果。使用AF和(hé)OCT數(shù)據計(jì)算(suàn)AF校(xiào)正因子将在最後一章解釋。
2. 實驗步驟
我們建立了一個(gè)能夠結合OCT和(hé)AF成像的雙态成像系統,OCT圖像測量Intralipid膜的厚度和(hé)濃度,AF圖像給出相應的AF信号強度。因此,AF-OCT成像可(kě)以映射不同濃度下AF強度和(hé)Intralipid厚度的關系。
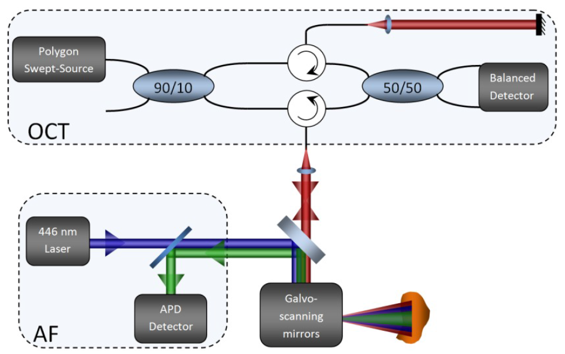
OCT光激發使用一個(gè)30mW基于多(duō)邊形掃描儀的掃描波長的激光光源,具有(yǒu)106.8nm的帶寬,中心波長為(wèi)1321.4nm。 激光光源為(wèi)一個(gè)基于光纖的具有(yǒu)參考臂和(hé)樣品臂的馬赫澤德幹涉儀(MZI),如圖1所示(OCT部分)。平衡的光電(diàn)探測器(qì)(ThorLabs)檢測幹涉。另一個(gè)MZI單元在光源處使用,來(lái)産生(shēng)樣品的參考時(shí)鍾。探測器(qì)輸出和(hé)MZI時(shí)鍾注入到數(shù)字轉換器(qì)卡(AlazarTech)中,實現信号處理(lǐ)和(hé)創建OCT圖像。
AF成像系統使用一個(gè)40mW的半導體(tǐ)激光器(qì)(相幹),在446nm處激發熒光。使用兩個(gè)1英寸直徑的透鏡和(hé)一個(gè)基于APD的探測器(qì)(Hamamatsu)來(lái)收集再發射的AF光子。二向色性的濾波片從AF光子中分離出後向散射的藍(lán)光,如圖1所示(AF部分)。通(tōng)過在自由空(kōng)間(jiān)的背面抛光寬闆電(diàn)介質反射鏡(ThorLabs),OCT和(hé)AF光信号可(kě)以實現結合和(hé)分離。電(diàn)流掃描鏡提供了樣品AF和(hé)OCT光束共同的2維掃描。
圖1.AF-OCT成像系統
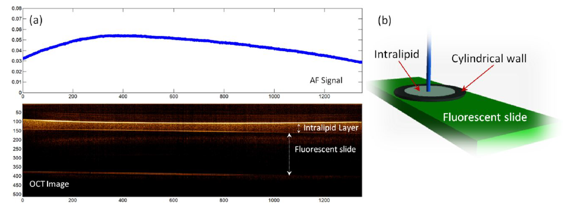
我們的模型,如圖2(b)所示,包括一個(gè)直徑為(wèi)1英寸的薄(1mm高(gāo))圓柱壁,它安裝在一個(gè)熒光載玻片上(shàng),以及圓柱壁中包圍着的Intralipid液體(tǐ)。改變容器(qì)中Intralipid的量會(huì)産生(shēng)不同的Intralipid膜厚度,由OCT圖像測得(de)。選擇封閉的圓柱壁時(shí),高(gāo)度要低(dī),直徑要大(dà),這樣就可(kě)以得(de)到小(xiǎo)的Intralipid膜厚度(μm範圍),同時(shí)在容器(qì)的中心區(qū)域可(kě)以接近扁平的表面以避免半月闆和(hé)透鏡效應。圖2(a)顯示了在熒光載玻片上(shàng)Intralipid膜的AF信号和(hé)OCT圖像。Intralipid膜的厚度和(hé)相對應的AF信号可(kě)以從圖中容易地獲得(de)。
圖2.(a)在熒光載玻片上(shàng)Intralipid膜的AF信号和(hé)OCT圖像,(b)Intralipid模型由在熒光載玻片上(shàng)的圓柱壁及其中包含的Intralipid組成。
3. 光線光學仿真
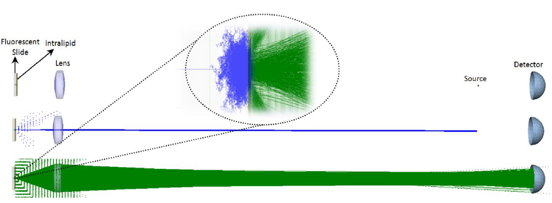
使用來(lái)自Photon Engineering公司的商業軟件包FRED,我們将實驗的結果與光線光學仿真的結果進行(xíng)比較。圖3顯示了仿真的配置和(hé)組件,包含一個(gè)藍(lán)色的激光光源(446nm)、一個(gè)熒光載玻片、一個(gè)Intralipid膜、用于聚焦藍(lán)光到樣品上(shàng)和(hé)收集重新發射的AF光子的1英寸透鏡(焦距40mm)、一個(gè)遠離透鏡50cm的探測器(qì),模仿實驗的裝置。探測器(qì)隻對大(dà)于500nm的波長敏感,以此分離AF光子和(hé)後向散射的藍(lán)光。
熒光載玻片由一個(gè)散射介質模拟,對于每個(gè)具有(yǒu)425nm–490nm波長範圍的入射光子,通(tōng)過散射介質的“平均自由程”後,散射介質會(huì)在随機方向重新發射一個(gè)550nm的光線。使用數(shù)量巨大(dà)的光線,重新發射光子的随機方向模仿由點光源産生(shēng)的球面波,等價于熒光輻射。平均自由程決定了入射光滲透到載玻片內(nèi)部的深度。Intralipid膜由具有(yǒu)各向異性(g)和(hé)散射系數(shù)((μs)的Henyey-Greenstein體(tǐ)散射模型來(lái)模拟。
圖3.包含一個(gè)熒光載玻片、一個(gè)Intralipid膜、一個(gè)1英寸透鏡、一個(gè)激光光源和(hé)一個(gè)探測器(qì)的光線光學仿真裝置。
4. 結果和(hé)討(tǎo)論
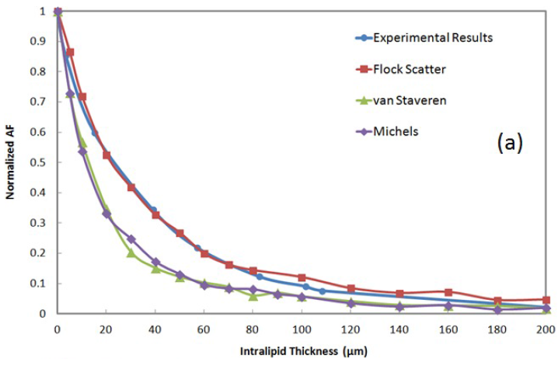
圖4(a)比較了10% Intralipid實驗結果和(hé)光線光學的仿真結果。Intralipid模型仿真需要散射參數(shù)(g, μs)。散射系數(shù)7-19的理(lǐ)論計(jì)算(suàn)和(hé)實驗測量在許多(duō)論文中已經提出。然而,文獻中報道(dào)的g和(hé)μs的值是變化的。我們使用在引用最多(duō)的文章中提出的數(shù)值來(lái)運行(xíng)仿真,也就是van Staveren, et al8、Michels, et al17和(hé)Flock, et al19。在實驗和(hé)仿真的情況下,所有(yǒu)的AF信号都歸一化沒有(yǒu)Intralipid膜的AF數(shù)值,來(lái)隔離Intralipid膜對AF信号的影(yǐng)響。使用由Flock, et al19給出的Intralipid散射參數(shù),我們實驗結果顯示出與仿真結果幾乎完美的匹配。然而,使用van Staveren, et al8和(hé)Michels, et al17提出的散射參數(shù),比我們實驗測量建議産生(shēng)了更多(duō)的AF損耗。
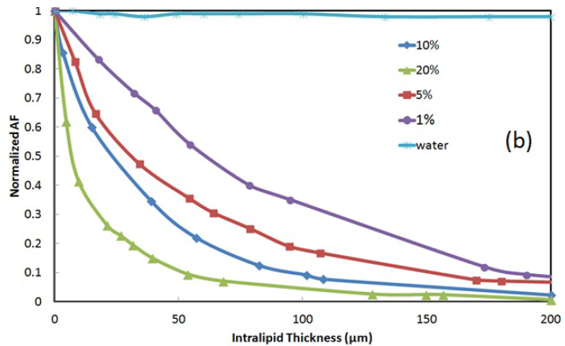
圖4.(a)AF信号随Intralipid厚度變化曲線,來(lái)自實驗(藍(lán)色圓)和(hé)對10%Intralipid使用由Flock(紅色方塊)、van Staveren(綠色三角)和(hé)Michels(紫色方塊)提出的散射參數(shù)的光線光學仿真,(b)對于不同的Intralipid濃度,實驗AF信号随Intralipid厚度變化曲線。
圖4(b)是對于不同的Intralipid濃度, 實驗AF信号随Intralipid厚度變化曲線。正如預期,20%的Intralipid會(huì)引起激發藍(lán)光的劇(jù)烈散射,重新發射AF會(huì)随着Intralipid厚度的增加急劇(jù)下降,然而,在較低(dī)的Intralipid濃度處,AF信号的損耗是比較少(shǎo)的。知道(dào)了Intralipid濃度,圖4(b)記錄了Intralipid膜引起的信号衰減,這可(kě)以用于AF校(xiào)正因子。因此給定一個(gè)Intralipid濃度,AF信号的校(xiào)正因子可(kě)以從圖4(b)中估計(jì)得(de)到。
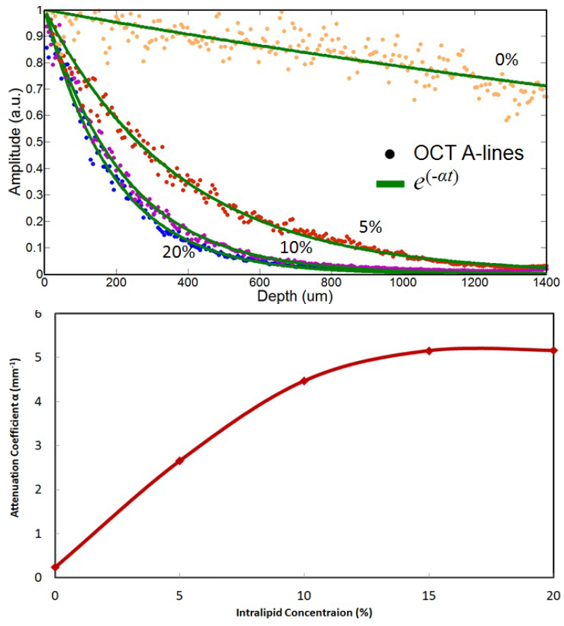
根據事實高(gāo)濃度會(huì)導緻嚴重的信号振幅的衰減,OCT A-scan數(shù)據可(kě)以給出Intralipid濃度,然而,對于低(dī)濃度這種衰減很(hěn)低(dī)。圖5(上(shàng))顯示了不同濃度下的OCT A-scan。A-scan數(shù)據(藍(lán)色圓)曲線拟合到e-at函數(shù)(綠色實線),産生(shēng)衰減系數(shù)(a)随Intralipid濃度的變化曲線,如圖5(下)所示。OCT數(shù)據可(kě)以測量散射顆粒(圖5b)的濃度,有(yǒu)助于找到圖4中對應的曲線。舉個(gè)例子,具有(yǒu)2.6mm-1OCT A-line損耗的樣品對應于大(dà)約5%的濃度的散射顆粒。因此,AF校(xiào)正因子可(kě)以由圖4(b)的紅色曲線确定。所以對于觀察到的AF信号,AF-OCT系統提供了足夠的信息來(lái)計(jì)算(suàn)校(xiào)正因子,從而可(kě)以用于減少(shǎo)較厚散射層引起的AF假陽性。
圖5.上(shàng):OCT A-line數(shù)據(圓)曲線拟合到e-at(綠色實線),下:從OCT A-line數(shù)據得(de)出的損耗系數(shù)a随Intralipid濃度的變化曲線。
5. 結論
我們進行(xíng)了一項Intralipid模型研究,使用組合的AF-OCT系統模拟了熒光介質上(shàng)覆蓋散射層的影(yǐng)響。對于不同的散射顆粒的濃度,呈現出随着散射層厚度變化的AF損耗曲線。OCT成像用于計(jì)算(suàn)散射層厚度和(hé)濃度,以及估計(jì)AF信号損耗所需的參數(shù)。模型用于從散射層引起的損耗計(jì)算(suàn)AF信号衰減的校(xiào)正因子。因此,結合AF-OCT系統能夠減少(shǎo)由于上(shàng)皮組織增厚引起的假陽性,增強AF疾病檢測的功效。
|